最新报道|CAR-T细胞治疗研发火热,专家集结分享探讨!
2019-11-13 00:00
2019年11月1日,Eppendorf 在深圳举办了一场以“细胞治疗技术研发与工艺”为主题的专业研讨会。
本次会议邀请了细胞治疗技术各个领域的专家,共话当前国内外 CAR-T 细胞治疗研发与产业化的机遇与挑战。

▲ Eppendorf 生物工艺中国区销售总监胡渺先生发表欢迎致辞
下面,小 E 就来分享一下,在本次会议上,专家们都探讨了哪些问题。
CAR-T 细胞治疗成药性研发
CAR 如何设计,从早期靶点确定,抗体发现,如何设计 scFV 判断,都是 CAR-T 细胞治疗最关键最核心。为此,来自科济生物医药(上海)有限公司抗体发现部门总监王鹏分享了如何基于 CAR-T 作用机制而进行的抗体设计,并提出了 CAR-T 成药性过程中需要注意哪些关键点。例如亲和力高低问题,并不是抗体筛选的时候,亲和力越高就越适合设计为 CAR;在早期研发设计 CAR 之前,建议做下 ScFv 是否存在聚集问题。

▲ 科济生物抗体发现部门总监王鹏
02
CAR -T 细胞治疗实体瘤的挑战
尽管 CAR-T 细胞在 B 细胞白血病和淋巴瘤中效果显著,但迄今为止尚未在实体肿瘤方面获得实质性进展,一些明显的制约因素影响着该疗法效能。
这些障碍主要包括:CAR-T 细胞的靶标问题;CAR-T 细胞运输不良或机体排斥导致的 CAR-T 细胞在肿瘤中积聚不足;浸润的 CAR-T 细胞暴露在具有免疫抑制的微环境中使这些细胞不能有效的发挥作用甚至出现凋亡。而归纳剖析这些现实来源的障碍,有助于重新设计下一代 CAR-T 细胞。
广州百暨基因科技有限公司首席技术官罗敏博士从实体瘤靶点选择、增强 CAR-T 迁移、克服肿瘤免疫抑制微环境和增加 CAR-T 增值存货四个方面介绍了 CAR-T 实体瘤临床进展与挑战。


最后,罗敏博士表示,目前上市的 CAR-T 疗法都非常昂贵,有统计显示,国内生产一批个体化 CAR-T 成本至少在 15 万人民币以上,那么通用型 CAR-T 或基因治疗产品有可能是未来降低成本趋势。

▲ 百暨基因首席技术官罗敏博士
03
CAR-T 细胞治疗工艺产业化技术
由于细胞治疗产品制备过程复杂、易变,目前监管和研发机构对其认知仍处在不断积累的过程中。
参照 CFDA《细胞治疗产品研究与评价技术指导原则(试行)》的要求,质粒和病毒载体作为 CAR-T 细胞生产的关键原材料直接关系到细胞产品的质量。质粒和病毒载体的生产应建立全过程的控制体系,包括原材料、生产工艺、关键点的质控、质粒和病毒载体的质量控制等,通过验证确保工艺的稳健性和批间一致性。
无锡生基医药科技有限公司产品开发部主任梁焯博士表示,在细胞、基因疗法产品生产过程中,污染与交叉污染风险相对传统生物制品更高,是 GMP 生产中最关键的质量风险。对于细胞治疗产品,初始原材料潜在含有各种病原,无法穷举验证,也无法通过筛选回避。因此 CAR-T 细胞的生产提倡封闭系统和一次性生产技术,避免交叉污染风险。

▲ 无锡生基产品开发部主任梁焯博士
深圳普瑞金生物药业有限公司药物工艺部经理蔡清华先生向参会听众详细介绍了质粒和慢病毒生产工艺开发流程和优化方法,通过悬浮 293T 细胞或贴壁细胞均可制备慢病毒原液。

▲ 病毒生产过程中 293T 细胞驯化悬浮培养技术

▲ 深圳普瑞金药物工艺部经理蔡清华先生
中山康晟生物技术有限公司 CEO 潘洪辉博士从 293 细胞分类,选择 239T 细胞的优势,贴壁驯化悬浮培养和开发 293 细胞培养基的详细情况等方面,全面介绍了有效提高 293 细胞包装病毒滴度培养基开发的解决方案。

▲ 康晟生物 CEO 潘洪辉博士
04
CAR-T 细胞治疗新型商业模式
李烈涛(Victor Li)医生凭借着丰富的行业经验,对于 CAR-T 疗法的商业模式有着独有见解。他认为知名科学家是一座宝库,并表示“通过产品授权、合作研发、提供种子资金等方式支持这些研究,我们可以挖掘出具有临床潜力的项目并进行孵化,最终通过转让或推进临床实现科研成果的产业转化。”

▲ 百吉生物创始人&总裁李烈涛博士
深圳宾德生物技术有限公司病毒研发总监刘婉博士从肿瘤免疫疗法历史、CAR-T 治疗国内外发展情况出发,介绍了宾德生物在 CAR-T 细胞治疗药物上的开发进展,同时分享了宾德在生物反应器上进行慢病毒制备的初次尝试。
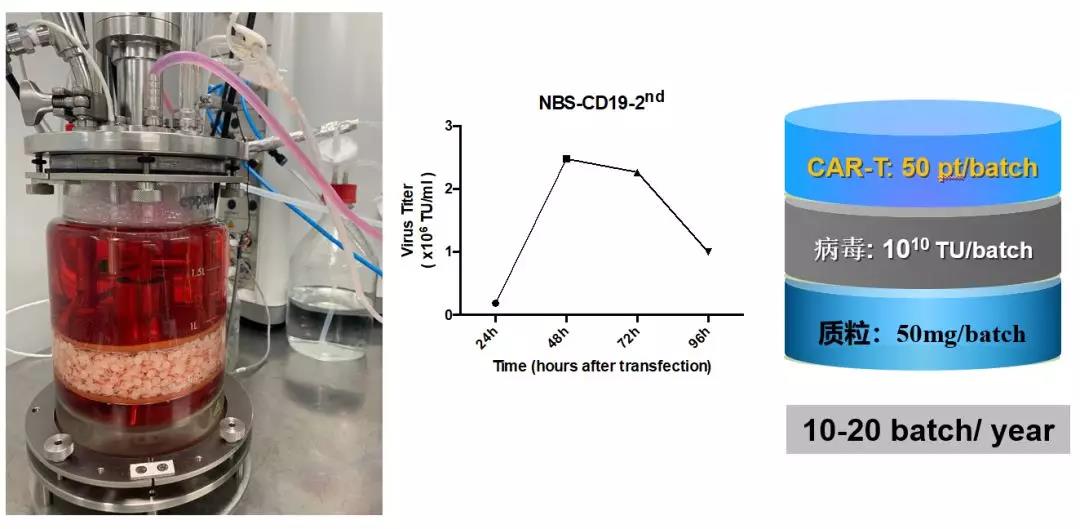
▲ 宾德公司慢病毒大规模制备的实验

▲ 宾德生物病毒研发总监刘婉博士
▼
东道主 Eppendorf 技术专家解正刚通过实际案例和数据向参会人员介绍了Eppendorf 产品在细胞治疗生物工艺中的部分质量控制和工艺流程解决方案。
PBMC (外周血单个核细胞)分离技术
采用离心机加速/减速等软刹车功能可在短时间内获得高产率、高纯度的 PBMC,减少样本损失。同时配备第三方认证的 Quick-Lock® 气密性转子盖以及气密性吊篮的离心机,在细胞分离中避免了交叉污染、样本外泄等生物危害。

▲ PBMC 密度梯度离心获得的结果(A/B/C/D为 5920 R 离心机,E 为其他品牌)

▲ Eppendorf 离心机系列转子
免疫细胞扩增解决方案
免疫细胞在静态培养中,可放置在稳定的 CO2 培养箱中。以 C170i 为例,该培养箱可以将选择 4 分或 8 分内门,避免不同来源细胞的交叉污染。
同时 C170i 可选铜制箱体,抑制细菌生长,并且可进行 180℃ 高温灭菌,有效避免培养中的污染风险。按照法规要求,设置三级权限管理,实时记录运行参数及事项,满足 GLP/GMP 的数据完整性规定。



▲ CellXpert® C170i 高温消毒 CO2 培养箱及 4/8 分内门
免疫细胞在动态悬浮培养中,可选择 S41i 摇床 CO2 培养箱。第一层可放置 T-flask 静态培养容器,第二层摇床可放置摇瓶或培养袋进行动态培养。
摇床和 CO2 培养箱一体化设计,避免了培养箱打孔等操作,减少污染率,以及 CO2 和热量的流失。摇床电机设计在箱体外,可保持箱体内温度的均一性和稳定性,也延长了湿热环境下摇床的使用寿命。包含摇床的培养箱可进行整体高温灭菌,满足合规要求。


▲ S41i 摇床 CO2 培养箱CO2 培养箱
慢病毒大规模制备解决方案
无论使用驯化的悬浮 293T 细胞还是贴壁的 293T 细胞,在制备慢病毒的过程中,如何提高病毒原液滴度和收获量,对工艺的设计是个不小的挑战。
Eppendorf 的 BioFlo® 320 系列生物反应器,既可以对驯化后的 293T 细胞进行大规模悬浮培养,也可通过篮式搅拌桨和片状载体,进行 293T 细胞的贴壁培养。两种方法都可以提高 293T 细胞的培养总量,为慢病毒大规模制备带来希望。
其中悬浮 293T 细胞在生物反应器内可达到 0.5-1.0x107个/ml;片状载体上贴壁的 293T 细胞更可达到 2.0-3.0x107个/ml。以贴壁 293T 细胞制备慢病毒为例,细胞在反应器内可增殖 50-100 倍,转染后,进行连续灌流收获,1.5L 工作体积的罐体可连续收获 8 天病毒液,6 个工作体积,高峰期病毒滴度达 3.0x108TU/ml。
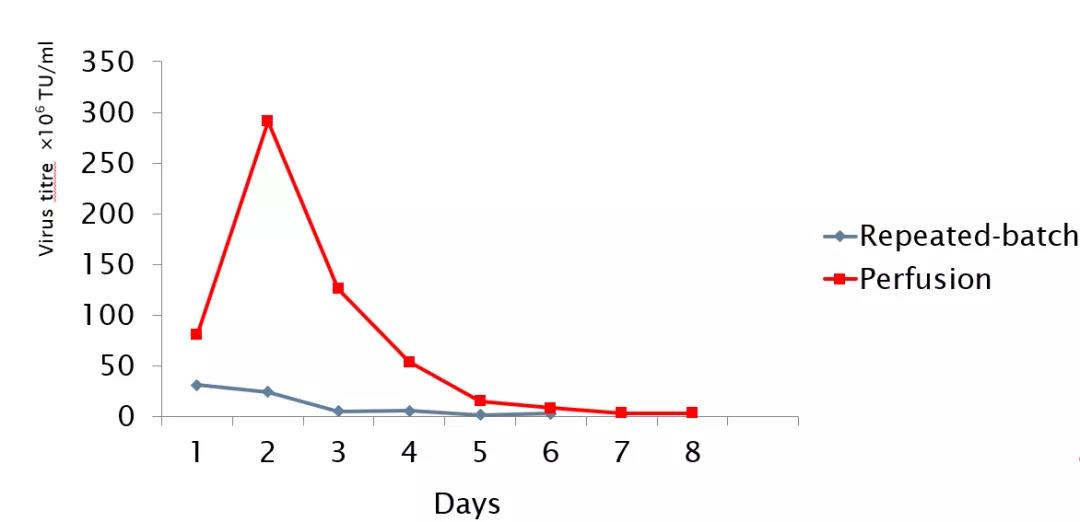 ▲ 慢病毒在生物反应器内的滴度曲线
▲ 慢病毒在生物反应器内的滴度曲线


▲ BioFlo® 320 反应器以及一次性 BioBlu 5p 罐体
Eppendorf 的 ep 和 Bioprocess 产品可以覆盖从细胞复苏开始到细胞成品或慢病原液的全部工艺流程。其中 BioFlo® 320 及其之后的一次性生物反应器 BioBlu 或 SIP 反应器均可提供符合 GMP 要求的 IQ、OQ 和各类验证文件。国内众多疫苗生产商、蛋白生产商、基因治疗药品生产商均选择了艾本德生物反应器,也证明了 Eppendorf 可以为细胞治疗领域研发及商业化工作提供强有力的保障。
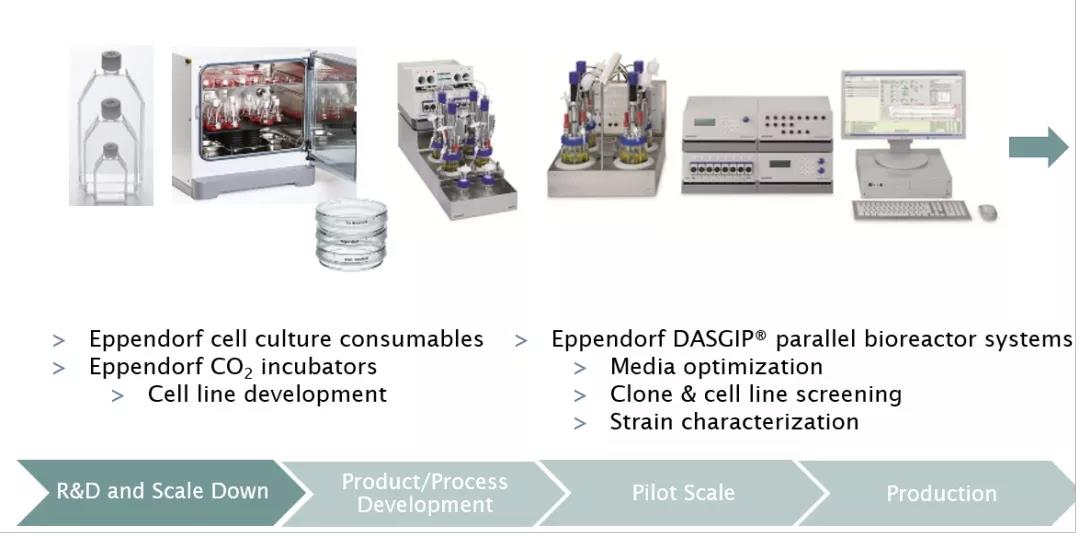


▲ Eppendorf 细胞培养工艺流程

▲ Eppendorf 技术专家解正刚先生
本次研讨会中,参会嘉宾还围绕抗体与 CAR-T 工程等基础研究、CAR-T 细胞治疗工艺开发与放大生产、质粒与病毒工艺开发与生产、293 细胞培养基开发等方向,进行了热烈讨论。


▲ 部分演讲嘉宾合影


